SPARK – Voies de signalisation et régulateurs des canaux K+
Chef d’équipe: Thomas Boulin — Site de l’équipe
C. elegans | excitabilité cellulaire | canaux potassiques | polarité cellulaire et tissulaire | maladies rares | neurobiologie moléculaire et cellulaire | édition dirigée du génome par CRISPR/Cas9
Thématiques de Recherche & Principaux Projets
Polarité et architecture membranaire des cellules musculaires de C. elegans
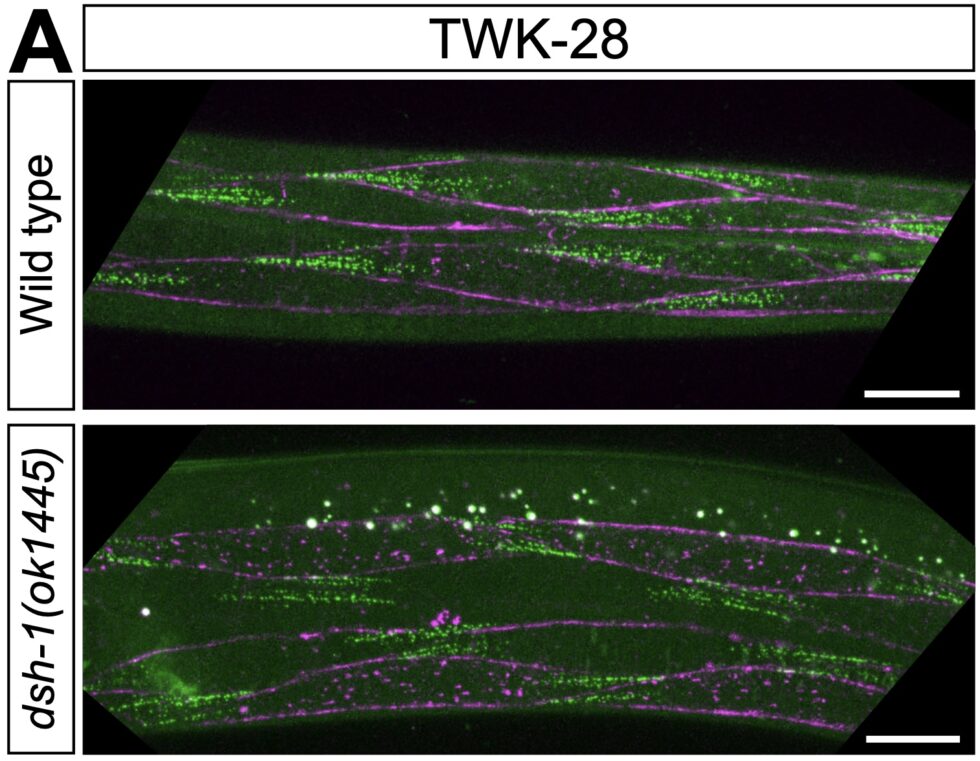
Les mécanismes de polarité cellulaire créent des domaines membranaires spécialisés, caractérisés par des compositions protéiques et des fonctions spécifiques. Par exemple, la plupart des canaux ioniques sont ciblés vers des compartiments bien définis au sein des cellules excitables. En analysant de manière systématique la localisation des canaux potassiques et d’autres protéines membranaires, nous avons récemment découvert que la membrane plasmique des cellules musculaires de C. elegans est polarisée (Peysson et al., Nature Communications, 2024).
Malgré nos connaissances approfondies du développement musculaire de C. elegans, cette forme remarquable de polarisation cellulaire était passée inaperçue. Elle ne repose pas sur les protéines classiques de la polarité planaire, mais sur une voie Wnt–Ror–Dvl non canonique, une voie de signalisation conservée et encore mal comprise, également impliquée dans la morphogenèse et le cancer. De plus, nous avons montré que le complexe protéique associé à la Dystrophine (DAPC) organise différents sous-compartiments membranaires au sein du sarcolemme.
Les questions clés auxquelles nous nous intéressons actuellement sont les suivantes :
(1) Quels sont les effecteurs en aval de la voie de signalisation Wnt–Ror–Dvl qui assurent la mise en place de la polarité musculaire ?
(2) Comment les différents domaines membranaires sont-ils établis et comment leur composition protéique spécifique est-elle déterminée ?
Analyse fonctionnelle de variants génétiques humains de canaux K⁺ et de protéines régulatrices impliqués dans les maladies rares neurodéveloppementales et cardiovasculaires


Les maladies humaines rares ne le sont que de nom : plus de 300 millions de personnes sont touchées par environ 7 000 de ces affections. Pour la plupart des patients, une longue odyssée diagnostique de plusieurs années reste la norme. Avec l’essor du séquençage génomique, les cliniciens identifient désormais facilement un nombre toujours croissant de variants génétiques. Alors que les variants fréquemment observés peuvent être interprétés facilement, les cas rares et les mutations faux-sens de novo demeurent particulièrement difficiles. Les études de validation fonctionnelle sont donc devenues essentielles pour déterminer la pathogénicité des variants identifiés chez des patients atteints de maladies génétiques rares.
Nous utilisons C. elegans comme système modèle pour valider fonctionnellement des variants de signification inconnue (VUS) dans des canaux potassiques et leurs protéines régulatrices, associés à des troubles neurodéveloppementaux rares et à des arythmies cardiaques héréditaires (Boulin et al., MGM 2021 ; Delinière et al., Journal of Physiology, 2025). En utilisant l’édition du génome par CRISPR/Cas9 et des tests phénotypiques, nous pouvons évaluer l’impact biologique de VUS dans un contexte cellulaire natif.
Menés en collaboration avec des cliniciens de l’Université Columbia (New York, USA) et du Centre National de Référence des Troubles du Rythme Cardiaque d’Origine Héréditaire de Lyon (CERA, HCL), ces projets relient notre recherche fondamentale à des applications cliniquement pertinentes. En combinant investigations cliniques et études moléculaires, cellulaires et sur organismes modèles, nous visons à résoudre les incertitudes diagnostiques et à élucider les mécanismes sous-jacents des maladies humaines rares.
Le syndrome du QT long congénital (LQTS) est une affection héréditaire pouvant entraîner une mort subite chez les jeunes individus. Avec une prévalence d’environ 1/2000 naissances, il s’agit de la canalopathie héréditaire la plus courante. Seize gènes sont associés au LQTS, et les variants du gène du canal potassique KCNH2 représentent à eux seuls 30 à 45 % des cas. KCNH2 code la sous-unité hERG du canal Kv11.1, qui porte le principal courant de repolarisation dans les cardiomyocytes. Une dysfonction du canal hERG prolonge la repolarisation et peut déclencher des arythmies ventriculaires fatales.
Nous avons récemment décrit les caractéristiques cliniques et électrophysiologiques du variant inédit KCNH2 p.Gly603Ser (Delinière et al., Gene 2024). Cette mutation chez un patient constitue le premier exemple d’un variant homozygote perte de fonction dans le pore de Kv11.1 provoquant un syndrome du QT long sévère mais viable, avec une expression clinique retardée.
Neurobeachin/NBEA est une protéine cérébrale de 327 kDa. La dysfonction de cette protéine est associée au syndrome NEDEGE (trouble neurodéveloppemental avec ou sans épilepsie généralisée à début précoce, OMIM 619157), une maladie neurologique très rare récemment identifiée. Neurobeachin est nécessaire au bon trafic de différentes classes de récepteurs de neurotransmetteurs chez les vertébrés. Nous avons découvert qu’elle est également requise pour la biosynthèse des canaux potassiques K2P chez le ver. En collaboration avec l’équipe de Tim Schedl (Washington University, St. Louis) et le Undiagnosed Diseases Network (UDN, NIH), nous avons développé le premier test fonctionnel pour les variants de NBEA sur la base de ces découvertes. Ce test a confirmé la pathogénicité d’un variant de novo identifié chez un patient pris en charge par l’UDN (Boulin et al., MGM 2021).
Pourquoi les individus diffèrent : déterminants génétiques, développementaux et environnementaux

Comprendre pourquoi les individus sont différents est une question fondamentale en biologie. En effet, des facteurs génétiques et non génétiques génèrent une variation phénotypique. Nous abordons cette question essentielle chez C. elegans en combinant des analyses computationnelles avec des approches expérimentales de biologie des systèmes. Nous nous concentrons particulièrement sur la dynamique de l’expression génique à l’échelle du génome — y compris au niveau d’une seule cellule ou d’un seul individu — en tant que phénotype intermédiaire multidimensionnel riche en information, et comme puissant moteur d’hypothèses mécanistiques. À cette fin, nous développons des méthodes informatiques permettant d’inférer et de quantifier précisément des phénotypes interprétables à partir de données -omiques, tels que l’âge physiologique (Bulteau et Francesconi, Nature Methods, 2022).
Grâce à ces stratégies, nous étudions comment l’expression des gènes est régulée dans l’espace (au niveau des tissus) et dans le temps (au cours du développement et du vieillissement). Nous explorons également pourquoi des individus génétiquement identiques diffèrent, en nous concentrant notamment sur l’impact de l’histoire développementale et de l’âge maternel sur la variation phénotypique. Enfin, nous étudions comment la perception sensorielle de l’environnement par une génération peut modifier le développement, le comportement et la fitness de la génération suivante, révélant ainsi des mécanismes de transmission d’information transgénérationnelle.
Façonner l’identité électrique des neurones de C. elegans – ETN Nervspan

Au cours du développement et du vieillissement, les neurones subissent une série de modifications morphologiques et fonctionnelles qui leur permettent d’établir puis de maintenir leur identité et leurs fonctions. Les récents progrès de la transcriptomique en cellule unique ont révélé que les différentes classes de neurones du système nerveux de C. elegans expriment des combinaisons spécifiques de canaux potassiques. Ces profils particuliers de canaux ioniques déterminent les propriétés biophysiques et électriques qui définissent les fonctions propres à chaque type de neurone tout au long de la vie de l’organisme.
Nous cherchons à comprendre :
(1) comment les différentes classes neuronales établissent leurs profils uniques d’expression des canaux potassiques ;
(2) par quels mécanismes cette identité électrique est maintenue au cours du temps ;
(3) et si elle peut être influencée par des perturbations externes ou modulée par des différences liées au sexe.
Actualités SPARK
New publication in The Journal of Physiology – Caenorhabditis elegans as an in vivo model system for human inherited primary arrhythmia syndromes
2025-12-05

Congratulations to Antoine for this expansive review!
Inherited primary arrhythmia syndromes (IPAS) are genetic heart diseases associated with an elevated risk of sudden cardiac death, particularly in young individuals. Modelling these rare and serious conditions is essential to elucidate their mechanisms and to identify new treatments.
Most genes involved in IPAS (e.g., congenital long-QT syndrome, catecholaminergic polymorphic ventricular tachycardia, calcium-release deficiency syndrome, Andersen-Tawil syndrome, Timothy syndrome, calmodulinopathies, and short-QT syndrome) are conserved in Caenorhabditis elegans, a model organism that offers powerful genetic tools for precise gene manipulation, including knock-in, knock-out, and knock-down approaches. In vivo studies in C. elegans can be used to characterize the consequences of genetic variants (at molecular, cellular, tissue, and behavioural scales), to identify new regulatory proteins, and to perform drug testing.
Here we summarize the characteristics of human IPAS and highlight the accumulating evidence that supports the utility of C. elegans as a simple yet powerful in vivo model for these diseases, capable of filling the gap between in vitro studies and complex transgenic animal models.
New publication in Brain Communications – Functional validation of human SK channels variants causing NEDMAB and Zimmermann–Laband syndrome-3 in C. elegans
2025-09-16

Congratulations to Sara for her first PhD publication!
Small conductance Ca2+-activated K+ channels (SK channels) are widely expressed in the central nervous system, where they play a crucial role in modulating neuronal excitability. Recent studies have identified missense variants in the genes encoding SK2 and SK3 channels as the cause of two rare neurodevelopmental disorders: NEDMAB and ZLS3, respectively.
Here, we used Caenorhabditis elegans as an in vivo model to investigate the functional consequences of these patient variants. The C. elegans orthologue KCNL-1 regulates neuronal and muscle excitability in the egg-laying system, a well-characterized model circuit. To visualize KCNL-1 expression and localization, we generated a fluorescent translational reporter at the endogenous kcnl-1 locus. We then introduced eight point mutations corresponding to pathogenic variants reported in NEDMAB or ZLS3 patients. Our study confirmed the molecular pathogenicity of the ZLS3-associated mutations, revealing a gain-of-function effect that led to increased in utero egg retention, likely due to electrical silencing of the egg-laying circuitry. NEDMAB mutations exhibited more complex phenotypic effects. Most caused a loss-of-function phenotype, indistinguishable from null mutants, while one displayed a clear gain-of-function effect. Additionally, a subset of NEDMAB variants altered KCNL-1 localization, suggesting an impairment in channel biosynthesis, trafficking or stability.
These findings provide new insights into the molecular mechanisms underlying NEDMAB and ZLS3 physiopathology, enhancing our understanding of SK channel dysfunction in human disease. Moreover, they establish C. elegans as a robust and cost-effective in vivo model for rapid functional validation of new SK channel mutations, paving the way for future investigations.
Félicitations Olga, élue membre junior de l’Institut universitaire de France !
2025-05-15

Par arrêté du ministre auprès de la ministre d’État, ministre de l’Éducation nationale, de l’Enseignement supérieur et de la Recherche, chargé de l’enseignement supérieur et de la recherche, en date du 15 mai 2025, Dr. Olga ANDRINI a été nommée membre Junior de l’IUF pour une durée de cinq ans à compter du 1er Octobre 2025.
Lauréate d’une chaire junior de l’Institut universitaire de France, elle ambitionne de mieux comprendre les bases moléculaires des canalopathies et de contribuer à l’interprétation fonctionnelle de variants génétiques rares.
New publication in PNAS – Constitutive sodium permeability in a C. elegans two-pore domain potassium channel.
2024-10-15

Congratulations to all involved in this multi-disciplinary exploration of the molecular determinants of K2P channel selectivity.
Potassium channels play a central role in modulating cellular excitability, particularly of neuronal cells. Their unique structure determines their ability to let ions pass selectively through cell membranes. The impact of pathological or evolutionary variations in this selectivity filter remains difficult to predict. Here, we reveal that UNC-58, a member of the two-pore domain potassium (K2P) channel family of C. elegans, exhibits an unusual sodium permeability due to a unique cysteine residue in its selectivity filter. Our findings underscore the importance of functional studies to determine how sequence variation in potassium channel selectivity filters can shape the electrical profiles of excitable cells.
New publication – Wnt-Ror-Dvl signalling and the dystrophin complex organize planar-polarized membrane compartments in C. elegans muscles
2024-06-10
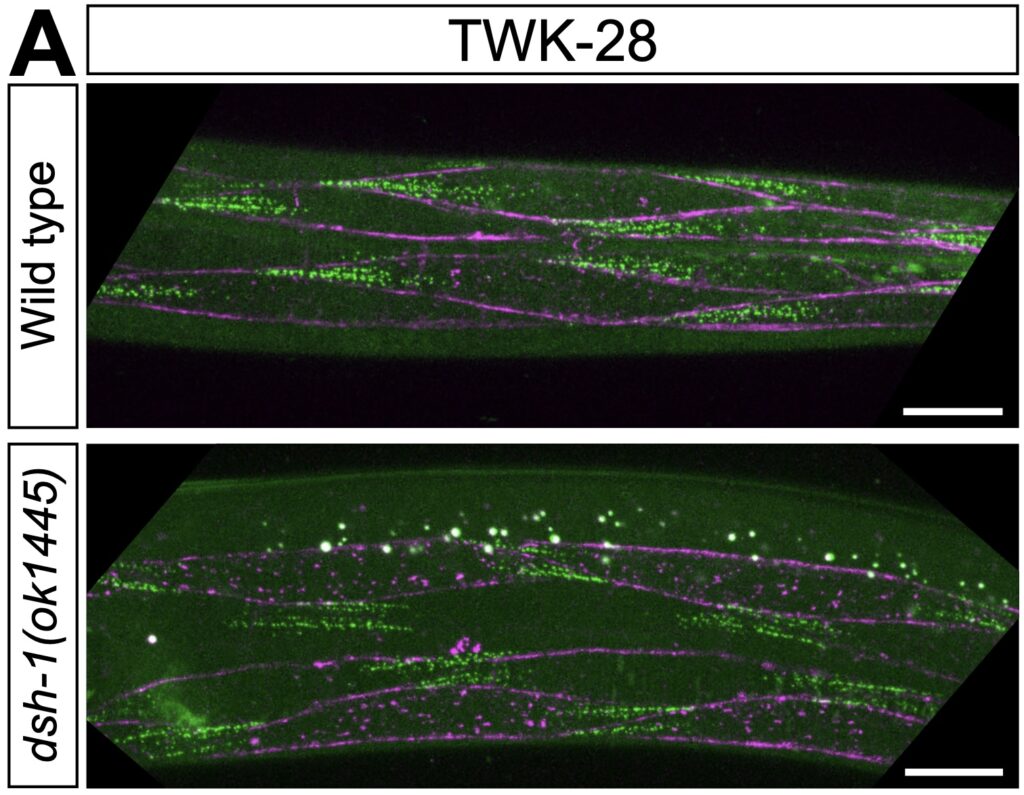
Our study revealing the remarkably complex organisation of the worm’s sarcolemma is now out at Nature Communications!
Almost six years in the making, congratulations to Alice, Nora, Marie, Amandine, Noémie, Elise and Olga for this magnum opus revealing this entirely unsuspected new case of planar cell polarity in C. elegans muscles.
SUMMARY
Cell polarity mechanisms allow the formation of specialized membrane domains with unique protein compositions, signalling properties, and functional characteristics. By analyzing the localization of potassium channels and proteins belonging to the dystrophin-associated protein complex, we reveal the existence of distinct planar-polarized membrane compartments at the surface of C. elegans muscle cells. We find that muscle polarity is controlled by a non-canonical Wnt signalling cascade involving the ligand EGL-20/Wnt, the receptor CAM-1/Ror, and the intracellular effector DSH-1/Dishevelled. Interestingly, classical planar cell polarity proteins are not required for this process. Using time-resolved protein degradation, we demonstrate that –while it is essentially in place by the end of embryogenesis– muscle polarity is a dynamic state, requiring continued presence of DSH-1 throughout post-embryonic life. Our results reveal the unsuspected complexity of the C. elegans muscle membrane and establish a genetically tractable model system to study cellular polarity and membrane compartmentalization in vivo.
New publication – Functional and clinical characterization of a novel homozygous KCNH2 missense variant in the pore region of Kv11.1 leading to a viable but severe long-QT syndrome
2023-12-21
Congratulations to Antoine, Olga and the team of Philippe Chevalier (Rhythmology department, HCL Lyon) for our first collaborative study about Kv11.1/hERG potassium channels.
Highlights
- Homozygous missense variants in the pore of Kv11.1 often lead to intrauterine death.
- We describe a novel hERG p.Gly603Ser homozygous loss-of-function variant.
- It causes a severe but viable long-QT syndrome with a delayed clinical expression.
- Family segregation and functional analysis classify hERG p.Gly603Ser as probably pathogenic.
DYSCO – Dystrophin-associated protein complex and subcellular compartmentalization
2023-07-13
Our project with the team of Vincent Mirouse (iGred, Clermont-Ferrand) and Helge Amthor (UVSQ) has been selected by ANR ! The Dystrophin Associated Protein Complex (DAPC) is a key actor of the cell – extracellular matrix (ECM) interface, as revealed by its implication in human genetic disorders. However, its molecular and cellular functions are still poorly understood because tractable model systems allowing state-of-the-art in vivo cell biology and genetic approaches are lacking. Our three teams have developed the first transgenic dystrophin reporters that have revealed remarkably compartmentalized membrane distributions of the DAPC in epithelia and muscle cells in C. elegans, Drosophila, and mouse. The project aims to elucidate the organization and dynamics of the DAPC and to characterize its new functions in relation to specific cell cortical compartments.
Fleggsibility – Dissecting the microevolutionary flexibility of a neural circuit
2022-08-13
Our project with the team of Christian Braendle (iBV Nice) and ViewPoint: Behavior Analysis Technologies has been selected by ANR ! On the heals of our joint publication (Vigne et al., Science Advances 2021) we will be trying to understand how specific neural circuits evolve to generate natural behavioural variation within species. In particular, the precise genetic changes that modulate cellular and developmental architectures of reproductive systems remain unclear. Here we will focus on the simple egg-laying circuit of the nematode Caenorhabditis elegans as a powerful model system to study natural microevolutionary (intraspecific) variability.
Rejoindre l’équipe
Domaine de recherche

Questions que nous souhaitons résoudre
- Quels sont les mécanismes cellulaires qui contrôlent la distribution des canaux K+ in vivo chez C. elegans ?
- Ces voies de régulation sont-elles conservées chez d’autres organismes, y compris les vertébrés ?
- Comment le nombre et l’activité des canaux K+ à la surface cellulaire sont-ils contrôlés ?
- Existe-t-il des facteurs spécifiques régulant différemment les canaux K+ selon les tissus ou les types cellulaires ?
- Les régulateurs des canaux K+ contrôlent-ils également la biologie d’autres familles de canaux ioniques ?
Études fonctionnelles des canaux potassiques à deux domaines pore (K2P) chez C. elegans

Les canaux potassiques jouent un rôle essentiel dans la régulation de l’excitabilité cellulaire, leur structure unique permettant le passage sélectif des ions à travers les membranes cellulaires. Les mutations gain de fonction qui modulent l’activité des canaux ioniques constituent des outils indispensables pour étudier leur fonction. Nous avons montré qu’un seul résidu conservé contrôle l’activité des canaux potassiques K2P chez les vertébrés et les invertébrés, et qu’il peut être muté de façon à augmenter progressivement la probabilité d’ouverture du canal (Ben Soussia et al., Nature Communications 2019). Cette découverte a été déterminante pour nos projets, car elle nous a permis de générer les lignées knock-in gain de fonction nécessaires à l’étude de la contribution des canaux K2P au contrôle de l’excitabilité cellulaire.
Trois études issues directement de ce travail ont été publiées. Deux études collaboratives décrivent le rôle du canal TWK-40 dans le contrôle de la locomotion et des comportements rythmiques (Yue et al., PNAS Nexus 2024 ; Meng et al., Science Advances 2024). Dans Meng et al., nous présentons un nouveau cadre conceptuel pour comprendre comment les animaux effectuent des transitions fluides entre des états moteurs opposés, tels que le déplacement en avant et en arrière. Dans la troisième étude, nous décrivons la caractérisation fonctionnelle d’un canal potassique atypique, UNC-58, qui constitue le premier exemple de canal K2P constitutivement perméable aux ions sodium (Andrini et al., PNAS 2024).
Variation évolutive du comportement de ponte chez C. elegans
Les comportements reproductifs varient considérablement chez les animaux — non seulement entre espèces, mais aussi au sein d’une même espèce. Cependant, notre compréhension des processus moléculaires permettant aux circuits neuronaux d’évoluer au sein d’une espèce pour générer une telle variation comportementale demeure limitée.
Nous avons utilisé le circuit de ponte de C. elegans comme système modèle pour étudier la variabilité microévolutive naturelle intraspécifique. En collaboration avec l’équipe de Christian Braendle (iBV, Nice), nous avons montré qu’une mutation dans un seul gène, le canal potassique SK KCNL-1, entraîne la perte de sensibilité environnementale chez plusieurs isolats naturels. Au lieu de réguler la ponte en fonction de la présence ou de l’absence de nourriture, ces isolats retiennent constitutivement leurs embryons, ce qui conduit à une éclosion interne. En combinant nos expertises complémentaires, nous avons obtenu une caractérisation complète — des niveaux moléculaire et cellulaire jusqu’au processus évolutif — ayant conduit à la sélection de ce phénotype paradoxal (Vigne et al., Science Advances 2021).
Dans le prolongement de ce travail, nous avons publié une seconde étude caractérisant la variation intraspécifique du comportement de ponte chez C. elegans (Mignerot et al., eLife 2023). Dans cette étude, en analysant une collection d’environ 300 isolats sauvages, nous décrivons une rétention intra-utérine fortement variable. En appliquant divers agents pharmacologiques et en manipulant génétiquement les niveaux endogènes de sérotonine chez 10 isolats sauvages, nous avons démontré que cette variation comportementale découle d’une architecture neuromodulatrice divergent au cours de l’évolution.
Membres de l’équipe
- Thomas BOULIN — CV — DR2 CNRS, HDR
- Olga ANDRINI CV — Maître de conférence, UCBL, HDR
- Antoine DELINIERE — Chercheur attaché MD, PhD, Hôpital Cardiologique, HCL
- Mirko FRANCESCONI CV— CRCN, Inserm, HDR
- Kathrin GIESELER — PREX, UCBL, HDR
- Sandra DUPERRIER — AI, CNRS
- Laura AGRESTI — Doctorante
- Parichitran AYYAMPERUMAL — Doctorant
- Clara BLANCFUNEY — Post-doc
- Élise CHEYNET — Doctorante
- Sara SECHI — Doctorante
- Minh Thu NGUYEN— Doctorante
Alumni
- Mélissa ZOUAK
- Claire LECROISEY
- Marie GENDREL
- Marine MERCIER
- Ismail BEN SOUSSIA
- Sonia EL MOURIDI
- Philippe TARDY
- Caroline BORKOWSKI
- Nora ZARIOHI
- Estèle LAFONT
- Alice LECLERCQ-BLONDEL
- Alice PEYSSON
- Guillaume BRULÈRE
Sélection de publications
Caenorhabditis elegans
as an
in vivo
model system for human inherited primary arrhythmia syndromes
Delinière A., Boulin T., Jospin M., et al.. 🔗 https://doi.org/10.1113/jp289661
Résumé :
Abstract Inherited primary arrhythmia syndromes (IPAS) are genetic heart diseases associated with an elevated risk of sudden cardiac death, particularly in young individuals. Modelling these rare and serious conditions is essential to elucidate their mechanisms and to identify new treatments. Most genes involved in IPAS (e.g., congenital long‐QT syndrome, catecholaminergic polymorphic ventricular tachycardia, calcium‐release deficiency syndrome, Andersen‐Tawil syndrome, Timothy syndrome, calmodulinopathies, and short‐QT syndrome) are conserved in Caenorhabditis elegans , a model organism that offers powerful genetic tools for precise gene manipulation, including knock‐in, knock‐out, and knock‐down approaches. In vivo studies in C. elegans can be used to characterize the consequences of genetic variants (at molecular, cellular, tissue, and behavioural scales), to identify new regulatory proteins, and to perform drug testing. Here we summarize the characteristics of human IPAS and highlight the accumulating evidence that supports the utility of C. elegans as a simple yet powerful in vivo model for these diseases, capable of filling the gap between in vitro studies and complex transgenic animal models. image
The Journal of Physiology , (2025)
Functional validation of human SK channels variants causing NEDMAB and Zimmermann–Laband syndrome-3 in C. elegans
Sechi S., Galaup C., Jospin M., et al.. 🔗 https://doi.org/10.1093/braincomms/fcaf351
Résumé :
Abstract Small conductance Ca2+-activated K+ channels (SK channels) are widely expressed in the central nervous system, where they play a crucial role in modulating neuronal excitability. Recent studies have identified missense variants in the genes encoding SK2 and SK3 channels as the cause of two rare neurodevelopmental disorders: NEDMAB and ZLS3, respectively. Here, we used Caenorhabditis elegans as an in vivo model to investigate the functional consequences of these patient variants. The C. elegans orthologue KCNL-1 regulates neuronal and muscle excitability in the egg-laying system, a well-characterized model circuit. To visualize KCNL-1 expression and localization, we generated a fluorescent translational reporter at the endogenous kcnl-1 locus. We then introduced eight point mutations corresponding to pathogenic variants reported in NEDMAB or ZLS3 patients. Our study confirmed the molecular pathogenicity of the ZLS3-associated mutations, revealing a gain-of-function effect that led to increased in utero egg retention, likely due to electrical silencing of the egg-laying circuitry. NEDMAB mutations exhibited more complex phenotypic effects. Most caused a loss-of-function phenotype, indistinguishable from null mutants, while one displayed a clear gain-of-function effect. Additionally, a subset of NEDMAB variants altered KCNL-1 localization, suggesting an impairment in channel biosynthesis, trafficking or stability. These findings provide new insights into the molecular mechanisms underlying NEDMAB and ZLS3 physiopathology, enhancing our understanding of SK channel dysfunction in human disease. Moreover, they establish C. elegans as a robust and cost-effective in vivo model for rapid functional validation of new SK channel mutations, paving the way for future investigations.
Brain Communications 7, (2025)
Constitutive sodium permeability in a
Caenorhabditis elegans
two-pore domain potassium channel
Andrini O., Ben Soussia I., Tardy P., et al.. 🔗 https://doi.org/10.1073/pnas.2400650121
Résumé :
Two-pore domain potassium (K2P) channels play a central role in modulating cellular excitability and neuronal function. The unique structure of the selectivity filter in K2P and other potassium channels determines their ability to allow the selective passage of potassium ions across cell membranes. The nematode C. elegans has one of the largest K2P families, with 47 subunit-coding genes. This remarkable expansion has been accompanied by the evolution of atypical selectivity filter sequences that diverge from the canonical TxGYG motif. Whether and how this sequence variation may impact the function of K2P channels has not been investigated so far. Here, we show that the UNC-58 K2P channel is constitutively permeable to sodium ions and that a cysteine residue in its selectivity filter is responsible for this atypical behavior. Indeed, by performing in vivo electrophysiological recordings and Ca 2+ imaging experiments, we demonstrate that UNC-58 has a depolarizing effect in muscles and sensory neurons. Consistently, unc-58 gain-of-function mutants are hypercontracted, unlike the relaxed phenotype observed in hyperactive mutants of many neuromuscular K2P channels. Finally, by combining molecular dynamics simulations with functional studies in Xenopus laevis oocytes, we show that the atypical cysteine residue plays a key role in the unconventional sodium permeability of UNC-58. As predicting the consequences of selectivity filter sequence variations in silico remains a major challenge, our study illustrates how functional experiments are essential to determine the contribution of such unusual potassium channels to the electrical profile of excitable cells.
Proceedings of the National Academy of Sciences 121, (2024)
Wnt-Ror-Dvl signalling and the dystrophin complex organize planar-polarized membrane compartments in C. elegans muscles
Peysson A., Zariohi N., Gendrel M., et al.. 🔗 https://doi.org/10.1038/s41467-024-49154-8
Résumé :
AbstractCell polarity mechanisms allow the formation of specialized membrane domains with unique protein compositions, signalling properties, and functional characteristics. By analyzing the localization of potassium channels and proteins belonging to the dystrophin-associated protein complex, we reveal the existence of distinct planar-polarized membrane compartments at the surface of C. elegans muscle cells. We find that muscle polarity is controlled by a non-canonical Wnt signalling cascade involving the ligand EGL-20/Wnt, the receptor CAM-1/Ror, and the intracellular effector DSH-1/Dishevelled. Interestingly, classical planar cell polarity proteins are not required for this process. Using time-resolved protein degradation, we demonstrate that –while it is essentially in place by the end of embryogenesis– muscle polarity is a dynamic state, requiring continued presence of DSH-1 throughout post-embryonic life. Our results reveal the unsuspected complexity of the C. elegans muscle membrane and establish a genetically tractable model system to study cellular polarity and membrane compartmentalization in vivo.
Nature Communications 15, (2024)
A tonically active master neuron modulates mutually exclusive motor states at two timescales
Meng J., Ahamed T., Yu B., et al.. 🔗 https://doi.org/10.1126/sciadv.adk0002
Résumé :
Continuity of behaviors requires animals to make smooth transitions between mutually exclusive behavioral states. Neural principles that govern these transitions are not well understood. Caenorhabditis elegans spontaneously switch between two opposite motor states, forward and backward movement, a phenomenon thought to reflect the reciprocal inhibition between interneurons AVB and AVA. Here, we report that spontaneous locomotion and their corresponding motor circuits are not separately controlled. AVA and AVB are neither functionally equivalent nor strictly reciprocally inhibitory. AVA, but not AVB, maintains a depolarized membrane potential. While AVA phasically inhibits the forward promoting interneuron AVB at a fast timescale, it maintains a tonic, extrasynaptic excitation on AVB over the longer timescale. We propose that AVA, with tonic and phasic activity of opposite polarities on different timescales, acts as a master neuron to break the symmetry between the underlying forward and backward motor circuits. This master neuron model offers a parsimonious solution for sustained locomotion consisted of mutually exclusive motor states.
Science Advances 10, (2024)
A leak K+ channel TWK-40 sustains the rhythmic motor program
Yue Z., Li Y., Yu B., et al.. 🔗 https://doi.org/10.1093/pnasnexus/pgae234
Résumé :
Abstract Leak potassium (K+) currents, conducted by two-pore domain K+ (K2P) channels, are critical for the stabilization of the membrane potential. The effect of K2P channels on motor rhythm remains enigmatic. We show here that the K2P TWK-40 contributes to the rhythmic defecation motor program (DMP) in Caenorhabditis elegans. Disrupting TWK-40 suppresses the expulsion defects of nlp-40 and aex-2 mutants. By contrast, a gain-of-function (gf) mutant of twk-40 significantly reduces the expulsion frequency per DMP cycle. In situ whole-cell patch clamping demonstrates that TWK-40 forms an outward current that hyperpolarize the resting membrane potential of dorsorectal ganglion ventral process B (DVB), an excitatory GABAergic motor neuron that activates expulsion muscle contraction. In addition, TWK-40 substantially contributes to the rhythmic activity of DVB. Specifically, DVB Ca2+ oscillations exhibit obvious defects in loss-of-function (lf) mutant of twk-40. Expression of TWK-40(gf) in DVB recapitulates the expulsion deficiency of the twk-40(gf) mutant, and inhibits DVB Ca2+ oscillations in both wild-type and twk-40(lf) animals. Moreover, DVB innervated enteric muscles also exhibit rhythmic Ca2+ defects in twk-40 mutants. In summary, these findings establish TWK-40 as a crucial neuronal stabilizer of DMP, linking leak K2P channels with rhythmic motor activity.
PNAS Nexus 3, (2024)
Functional analysis of a de novo variant in the neurodevelopment and generalized epilepsy disease gene NBEA
Boulin T., Itani O., El Mouridi S., et al.. 🔗 https://doi.org/10.1016/j.ymgme.2021.07.013
Résumé :
Résumé non disponible.
Molecular Genetics and Metabolism 134, 195-202 (2021)
A single-nucleotide change underlies the genetic assimilation of a plastic trait
Vigne P., Gimond C., Ferrari C., et al.. 🔗 https://doi.org/10.1126/sciadv.abd9941
Résumé :
A single-nucleotide change underlies the transition from environmentally induced to genetically encoded matricidal hatching.
Science Advances 7, (2021)
Mutation of a single residue promotes gating of vertebrate and invertebrate two-pore domain potassium channels
Ben Soussia I., El Mouridi S., Kang D., et al.. 🔗 https://doi.org/10.1038/s41467-019-08710-3
Résumé :
AbstractMutations that modulate the activity of ion channels are essential tools to understand the biophysical determinants that control their gating. Here, we reveal the conserved role played by a single amino acid position (TM2.6) located in the second transmembrane domain of two-pore domain potassium (K2P) channels. Mutations of TM2.6 to aspartate or asparagine increase channel activity for all vertebrate K2P channels. Using two-electrode voltage-clamp and single-channel recording techniques, we find that mutation of TM2.6 promotes channel gating via the selectivity filter gate and increases single channel open probability. Furthermore, channel gating can be progressively tuned by using different amino acid substitutions. Finally, we show that the role of TM2.6 was conserved during evolution by rationally designing gain-of-function mutations in four Caenorhabditis elegans K2P channels using CRISPR/Cas9 gene editing. This study thus describes a simple and powerful strategy to systematically manipulate the activity of an entire family of potassium channels.
Nature Communications 10, (2019)
Financements et soutien
2023-2027 MSCA European Doctoral Network — « NERVSPAN – Molecular plasticity of neurons during C. elegans lifespan »
2023-2028 Agence Nationale de la Recherche — « DYSCO – Dystrophin-associated protein complex and subcellular compartmentalization »
2022-2026 Agence Nationale de la Recherche — « Fleggsibility – Dissecting the microevolutionary flexibility of a neural circuit »
2020-2025 Agence Nationale de la Recherche — « NBelegAns – Molecular, cellular, and clinical investigation of the autism, epilepsy, and neurodevelopmental disorder gene Neurobeachin/NBEA »
2020-2025 Labex CORTEX website
2016-2021 AFM Téléthon — Alliance MyoNeurALP
2019-2020 Fondation Maladies Rares — « Modeling disease-causing mutations of Neurobeachin/NBEA in the nematode Caenorhabditis elegans »
2013-2019 European Research Council — Kelegans — « Genetics and cell biology of K2P channels »
2013-2014 Fondation Fyssen













